Das glymphatische System Ihres Gehirns ist mehr als nur eine passives Leitungsnetz.
Your brain’s glymphatic system is more than passive plumbing
In der Neurologie kommen wir langsam zu einer Erkenntnis, die Menschen mit Erkrankungen und Pflegekräfte schon seit Jahrzehnten spüren: Schlaf ist kein Luxus und keine Option. Er ist eine biologische Notwendigkeit, die still und leise dafür sorgt, dass sich das Gehirn regeneriert, Abfallstoffe beseitigt und seine Funktionen über lange Zeit hinweg aufrechterhält. Nirgendwo wird dies deutlicher als bei der Parkinson-Krankheit, einer Erkrankung, die lange Zeit mit dem Verlust von Dopamin in Verbindung gebracht wurde, aber zunehmend als eine biologisch bedingte Störung des gesamten Gehirns und des gesamten Körpers verstanden wird, die sich über Jahrzehnte hinweg entwickelt.
Das Aufkommen des glymphatischen Systems hat uns einen Rahmen geboten, um zu verstehen, warum Schlaf so wichtig ist. Das glymphatische Netzwerk zirkuliert die Gehirn-Rückenmarks-Flüssigkeit durch perivaskuläre Räume und erleichtert so die Beseitigung von Stoffwechselabfällen, fehlgefalteten Proteinen und entzündlichen Nebenprodukten aus dem Gehirn. Während des Schlafs, insbesondere im Slow-Wave-Schlaf, wird dieses System deutlich aktiver. Der extrazelluläre Raum dehnt sich aus, die Flüssigkeitsbewegung nimmt zu und die Ausscheidung beschleunigt sich.
Im Wesentlichen öffnet der Schlaf das Reinigungssystem des Gehirns und ermöglicht es ihm, sich für den nächsten Tag zurückzusetzen.
Wenn der Schlaf fragmentiert, verkürzt oder gestört ist, gerät dieses System ins Stocken und es sammeln sich Abfallstoffe an.
Dies ist für die Parkinson-Krankheit von großer Bedeutung. Das pathologische Kennzeichen von Parkinson ist die Ansammlung und Ausbreitung von fehlgefalteten Alpha-Synucleinen. Während wir uns oft auf Neuronen, Synapsen und Schaltkreise konzentrieren, existieren diese Proteine in einem Ökosystem, das von Reinigungsmechanismen abhängt, die für die Erhaltung der Gesundheit entscheidend sind.
Experimentelle und klinische Daten deuten nun darauf hin, dass eine beeinträchtigte glymphatische Funktion die Fähigkeit des Gehirns zur Beseitigung toxischer Proteine verringern kann, insbesondere mit zunehmendem Alter. Der Slow-Wave-Schlaf scheint ein kritisches Zeitfenster zu sein, in dem diese Clearance am effizientesten ist. Wenn sich dieses Zeitfenster verengt, kann sich die Pathologie ausbreiten.
Seit mehr als einem Jahrzehnt zeigen Forschungsarbeiten, dass der glymphatische Transport kein passiver Transportvorgang ist, sondern ein regulierter, zustandsabhängiger biologischer Prozess, der mit Schlaf, zirkadianen Rhythmen, Gefäßpulsation, Atmung und astroglialen Wasserkanälen wie Aquaporin-4 zusammenhängt.
Wichtig ist, dass die glymphatische Clearance mit zunehmendem Alter nachlässt und anfällig für Gefäßerkrankungen, Schlafentzug, circadiane Störungen und Neurodegeneration selbst ist.
In Tiermodellen für Parkinson wurde eine Verlängerung des Slow-Wave-Schlafs mit einer verringerten Alpha-Synuclein-Akkumulation und einer verbesserten glymphatischen Funktion in Verbindung gebracht, was darauf hindeutet, dass Schlaf ein veränderbarer Hebel sein könnte und nicht nur eine unvermeidliche Begleiterscheinung des Krankheitsverlaufs.
Jahrelang wurden Schlafstörungen bei Parkinson in erster Linie als zu behandelnde Symptome betrachtet. REM-Schlafverhaltensstörungen, Schlaflosigkeit, übermäßige Tagesmüdigkeit, Schlafapnoe und circadiane Fehlausrichtung wurden katalogisiert, stückweise behandelt und oft zugunsten der Kontrolle motorischer Symptome zurückgestellt. Dieser Ansatz erscheint heute überholt.
Wenn Schlaf eines der wichtigsten Instrumente des Gehirns für die Abfallbeseitigung, die Immunregulation und die synaptische Homöostase ist, dann könnte eine chronische Schlafstörung ein Treiber der Krankheitsbiologie sein und nicht nur ein Nebenprodukt.
Diese Erkenntnis sollte einen Wandel hin zu einer präventiven Neurologie erzwingen. Parkinson beginnt nicht mit Tremor. Es entwickelt sich still und leise, Jahre vor der Diagnose, in einer Phase, in der häufig Schlafstörungen auftreten, die jedoch unterschätzt werden. Die REM-Schlafverhaltensstörung beispielsweise ist einer der stärksten klinischen Prädiktoren für zukünftige Synucleinopathien. Anstatt dies als unvermeidlich anzusehen, wirft das glymphatische Konzept eine andere Frage auf:
Kann die frühzeitige Erkennung und der Schutz der Schlafphysiologie den Krankheitsverlauf verlangsamen oder verändern?
Die Auswirkungen gehen über die individuelle Versorgung hinaus. Unser Gesundheitssystem ist reaktiv, fragmentiert und schlecht darauf ausgelegt, den Schlaf zu schützen.
Wir normalisieren Schlafentzug, belohnen Produktivität statt Erholung und behandeln Schlafstörungen als zweitrangig. Bei der Parkinson-Krankheit ist dies besonders kostspielig. Schlechter Schlaf verschlechtert motorische Symptome, Kognition, Stimmung, autonome Funktionen und erhöht natürlich die Belastung für Pflegekräfte. Er erhöht das Sturzrisiko, beschleunigt den Funktionsverlust und beeinträchtigt die Lebensqualität. Dennoch wird die Schlafversorgung nach wie vor isoliert, uneinheitlich bewertet und selten in die langfristige Krankheitsplanung integriert.
Hier kommt das Parkinson’s Universe-Modell ins Spiel. Schlaf kann nicht isoliert optimiert werden. Er erfordert eine Koordinierung zwischen Neurologie, Primärversorgung, Schlafmedizin, psychischer Gesundheit und Rehabilitation und benötigt die Unterstützung der Pflegekräfte. Medikamente müssen auf Schlafstörungen überprüft werden. Circadiane Signale müssen beachtet werden. Schlafapnoe muss erkannt und behandelt werden. REM-Schlafverhaltensstörungen müssen frühzeitig erkannt werden. Technologie kann dabei helfen, Schlafmuster zu überwachen, aber erst Beziehungen und koordinierte Teams setzen Daten in Maßnahmen um. Schlaf ist keine einzelne Intervention, sondern ein Problem des gesamten Ökosystems.
Daraus lässt sich auch eine allgemeinere Lehre für die öffentliche Gesundheit ziehen. Die glymphatische Biologie erinnert uns daran, dass Prävention keine Pille ist. Es ist ein Plan. Schlaf steht in Zusammenhang mit Herz-Kreislauf-Gesundheit, Stoffwechselerkrankungen, Umwelteinflüssen und sozialen Determinanten. Bluthochdruck, Diabetes und Gefäßerkrankungen beeinträchtigen ebenfalls den glymphatischen Fluss. Schichtarbeit und circadiane Störungen verändern die Clearance-Rhythmen. Eine Atemwegsobstruktion während des Schlafs kann die intrakranielle oder „Dynamik im Gehirn“ verändern. Dies sind keine Nischenprobleme, sondern Probleme auf Bevölkerungsebene, die die Gesundheit des Gehirns während des gesamten Lebens beeinflussen.
Wir haben bereits gesehen, dass dieses Vorgehen erfolgreich ist. HIV und Brustkrebs haben uns gelehrt, dass sich die Ergebnisse ändern, wenn wir in Früherkennung, Prävention, koordinierte Versorgung und nachhaltige Forschung investieren. Parkinson verdient die gleiche Dringlichkeit.
Der Schutz des Schlafs und der glymphatischen Funktion kann Parkinson vielleicht nicht heilen, aber es kann den Ausbruch verzögern, das Fortschreiten verlangsamen und die Belastung auf eine Weise verringern, die mit Pharmakologie allein nicht erreicht werden kann.
Die Wissenschaft entwickelt sich noch weiter, und Bescheidenheit ist angebracht. Die glymphatische Biologie ist komplex, und es bleiben noch viele Fragen zu Messung, Kausalität und Übertragung auf den Menschen offen. Die Richtung ist klar. Schlaf ist nicht nebensächlich für die Gesundheit des Gehirns. Er ist grundlegend. Wenn wir dies weiterhin ignorieren, tun wir dies auf eigene Gefahr.
Parkinson sollte uns dazu zwingen, anders zu denken, nicht nur in Bezug auf die Behandlung, sondern auch in Bezug auf die Zeit. Was wir Jahre vor der Diagnose tun, ist wichtig. Wie wir schlafen, ist wichtig. Und ob wir Systeme entwickeln, die die Fähigkeit des Gehirns zur Reinigung, Reparatur und Regeneration schützen, könnte letztendlich darüber entscheiden, ob wir die Kurve dieser wachsenden neurologischen Pandemie abflachen können.
Referenzen:
Can we Bend the Curve of Parkinson’s Disease by Improving Our Sleep?
Across neurology, we are slowly coming to terms with a truth that persons with disease and caregivers have both sensed for decades: sleep is not a luxury, and it is not optional. It is a biological necessity that quietly governs how the brain repairs itself, clears waste and preserves function over time. Nowhere is this becoming more evident than in Parkinson’s disease, a condition long framed around dopamine loss, but increasingly understood as a whole-brain, whole-body disorder shaped by biology that unfolds across decades.
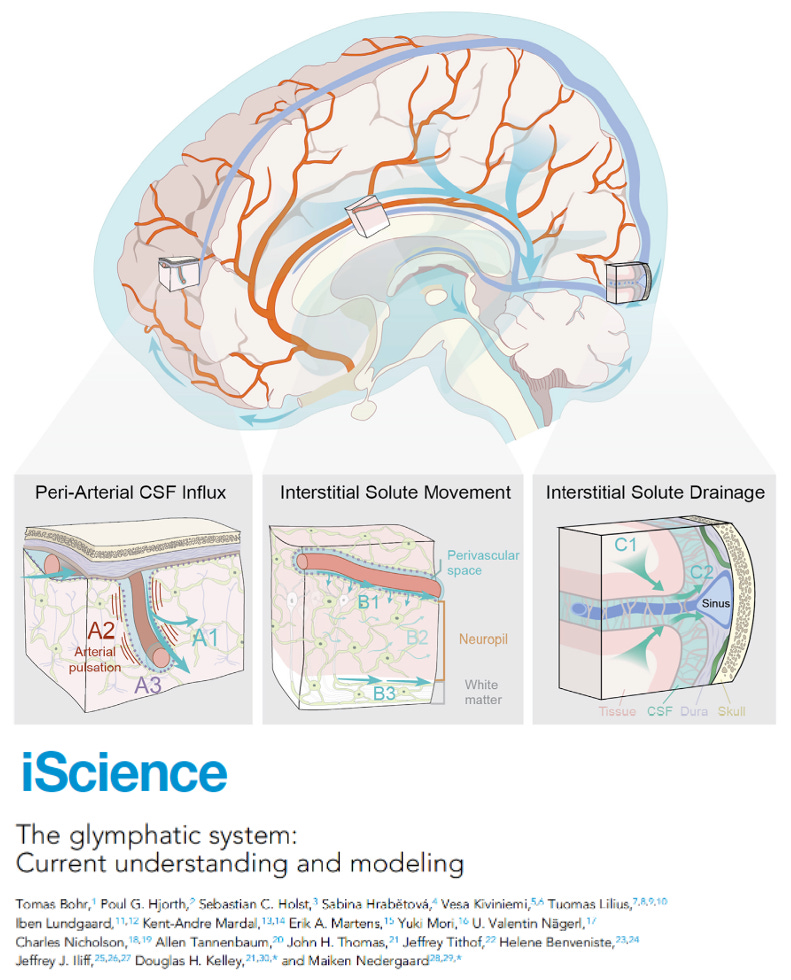
The emergence of the glymphatic system has offered us a framework to understand why sleep matters so profoundly. The glymphatic network circulates cerebrospinal fluid through perivascular spaces, facilitating the clearance of metabolic waste, misfolded proteins and inflammatory byproducts from the brain. During sleep, particularly slow-wave sleep, this system becomes markedly more active. The extracellular space expands, fluid movement increases, and clearance accelerates. In essence, sleep opens the sanitation system of the brain, allowing it to reset for the next day. When sleep is fragmented, shortened, or disrupted, that system falters, and waste accumulates.
This matters deeply for Parkinson’s disease. The pathological hallmark of Parkinson’s is the accumulation and spread of misfolded alpha-synuclein. While we often focus on neurons, synapses, and circuits, these proteins exist within an ecosystem that depends on clearance mechanisms crucial to remaining healthy. Experimental and clinical data now suggest that impaired glymphatic function may reduce the brain’s ability to clear toxic proteins, particularly as we age. Slow-wave sleep appears to be a critical window during which this clearance is most efficient. When that window narrows, pathology may gain a foothold.
There is now more than a decade of work showing that glymphatic transport is not passive plumbing, but a regulated, state-dependent biological process tied to sleep, circadian rhythms, vascular pulsatility, respiration and astroglial water channels such as aquaporin-4. Importantly, glymphatic clearance slows with aging and is vulnerable to vascular disease, sleep deprivation, circadian disruption and to neurodegeneration itself. In animal models of Parkinson’s, enhancing slow-wave sleep over time has been associated with reduced alpha-synuclein accumulation and improved glymphatic function, suggesting that sleep may be a modifiable lever, rather than a fixed casualty of disease progression.
For years, sleep disturbances in Parkinson’s were viewed primarily as symptoms to manage. REM sleep behavior disorder, insomnia, excessive daytime sleepiness, sleep apnea and circadian misalignment were cataloged, treated piecemeal, and often deprioritized in favor of motor symptom control. That approach now feels outdated. If sleep is one of the brain’s primary tools for waste clearance, immune regulation and for synaptic homeostasis, then chronic sleep disruption may be a driver of disease biology, not merely a byproduct.
This realization should force a shift toward preventive neurology. Parkinson’s does not begin with tremor. It unfolds silently, years before diagnosis, during a phase when sleep disruption is frequently present, however underappreciated. REM sleep behavior disorder, for example, is one of the strongest clinical predictors of future synucleinopathies. Rather than viewing this as an inevitability, the glymphatic framework invites a different question: can early identification and protection of sleep physiology slow or alter disease trajectories?
The implications extend beyond individual care. Our health care system is reactive, fragmented, and poorly designed to protect sleep. We normalize sleep deprivation, reward productivity over recovery, and treat sleep disorders as secondary concerns. In Parkinson’s disease, this is particularly costly. Poor sleep worsens motor symptoms, cognition, mood, autonomic function and of course fuels caregiver strain. It increases fall risk, accelerates functional decline and erodes quality of life. Yet sleep care remains siloed, inconsistently assessed, and rarely integrated into long-term disease planning.
This is where the Parkinson’s Universe model becomes relevant. Sleep cannot be optimized in isolation. It requires coordination across neurology, primary care, sleep medicine, mental health, rehabilitation and it will require caregiver support. Medications must be reviewed for sleep disruption. Circadian cues must be respected. Sleep apnea must be identified and treated. REM sleep behavior disorder must be recognized early. Technology can help to monitor sleep patterns, however relationships and coordinated teams are what will turn data into action. Sleep is not a single intervention; it is an ecosystem problem.
There is also a broader public health lesson. Glymphatic biology reminds us that prevention is not a pill. It is a plan. Sleep intersects with cardiovascular health, metabolic disease, environmental exposures and social determinants. Hypertension, diabetes and vascular disease also impair glymphatic flow. Shift work and circadian disruption alter clearance rhythms. Airway obstruction during sleep can changes intracranial or ‘inside the brain dynamics.’ These are not niche concerns; they are population-level issues that shape brain health across the lifespan.
We have seen this playbook succeed before. HIV and breast cancer taught us that outcomes change when we invest in early detection, prevention, coordinated care and sustained research. Parkinson’s deserves the same urgency. Protecting sleep and glymphatic function may not cure Parkinson’s, but it may delay onset, slow progression and reduce burden in ways that pharmacology alone has not achieved.
The science is still evolving, and humility is warranted. Glymphatic biology is complex, and many questions remain about measurement, causality, and translation to humans. The direction is clear. Sleep is not ancillary to brain health. It is foundational. If we continue to ignore it, we do so at our peril.
Parkinson’s should force us to think differently, not just about treatment, but about time. What we do years before diagnosis matters. How we sleep matters. And whether we design systems that protect the brain’s ability to clean, repair and to recover may ultimately determine whether we bend the curve of this growing neurological pandemic.
References:
1. Lv Y, Ding XS, Gao L, et al. Glymphatic dysfunction in Parkinson’s disease: Aging-associated impairments, imaging biomarkers, and therapeutic strategies. Ageing Res Rev 2026; 114: 102995.
2. Lian X, Liu Z, Gan Z, et al. Targeting the glymphatic system to promote alpha-synuclein clearance: a novel therapeutic strategy for Parkinson’s disease. Neural Regen Res 2026; 21(1): 233-47.
3. Wang S, Wu D, Chen G, et al. Agomelatine Targets Aquaporin-4 Polarization to Rescue Glymphatic Dysfunction in Parkinson’s Disease. Neurosci Bull 2025.
4. Urso D, Gnoni V, Rollo E, Santoro C, Jost WH, Logroscino G. The Glymphatic System and Sleep Dysfunction in Parkinson’s Disease. Sleep Med Clin 2025; 20(3): 379-87.
5. Rajai Firouzabadi S, Mohammadi I, Aghajanian S, et al. Glymphatic Dysfunction in Parkinson’s Disease: A Systematic Review and Meta-Analysis of Neuroimaging Studies. Mov Disord Clin Pract 2025.
6. Okun MS, Bloem BR, Dorsey ER. The Parkinson’s Universe: A person-centered care model for Parkinson’s disease. J Parkinsons Dis 2025: 1877718X251399958.
7. Nepozitek J, Sonka K. Obstructive sleep apnea as a possible mediator for the association between glymphatic function and body mass index in Parkinson’s disease. Quant Imaging Med Surg 2025; 15(8): 7674-5.
8. Nepozitek J, Marecek S, Rottova V, et al. Glymphatic dysfunction evidenced by DTI-ALPS is related to obstructive sleep apnea intensity in newly diagnosed Parkinson’s disease. NPJ Parkinsons Dis 2025; 11(1): 160.
9. Nepozitek J, Dusek P, Sonka K. Glymphatic system, sleep, and Parkinson’s disease: interconnections, research opportunities, and potential for disease modification. Sleep 2025; 48(1).
10. Ma X, Liu Y, Xie M, et al. Parkinson’s disease with possible REM sleep behavior disorder correlated with more severe glymphatic system dysfunction. NPJ Parkinsons Dis 2025; 11(1): 82.
11. Li Y, Zhang T, Wang C, et al. The Impact of Sleep Disorders on Glymphatic Function in Parkinson’s Disease Using Diffusion Tensor MRI. Acad Radiol 2025; 32(4): 2209-19.
12. Yue Y, Zhang X, Lv W, Lai HY, Shen T. Interplay between the glymphatic system and neurotoxic proteins in Parkinson’s disease and related disorders: current knowledge and future directions. Neural Regen Res 2024; 19(9): 1973-80.
13. Gui Q, Meng J, Shen M, et al. Relationship of Glymphatic Function with Cognitive Impairment, Sleep Disorders, Anxiety and Depression in Patients with Parkinson’s Disease. Neuropsychiatr Dis Treat 2024; 20: 1809-21.
14. Cai X, Chen Z, He C, et al. Diffusion along perivascular spaces provides evidence interlinking compromised glymphatic function with aging in Parkinson’s disease. CNS Neurosci Ther 2023; 29(1): 111-21.
15. Si X, Guo T, Wang Z, et al. Neuroimaging evidence of glymphatic system dysfunction in possible REM sleep behavior disorder and Parkinson’s disease. NPJ Parkinsons Dis 2022; 8(1): 54.
16. Scott-Massey A, Boag MK, Magnier A, Bispo D, Khoo T, Pountney DL. Glymphatic System Dysfunction and Sleep Disturbance May Contribute to the Pathogenesis and Progression of Parkinson’s Disease. Int J Mol Sci 2022; 23(21).
17. Buccellato FR, D’Anca M, Serpente M, Arighi A, Galimberti D. The Role of Glymphatic System in Alzheimer’s and Parkinson’s Disease Pathogenesis. Biomedicines 2022; 10(9).
18. Sundaram S, Hughes RL, Peterson E, et al. Establishing a framework for neuropathological correlates and glymphatic system functioning in Parkinson’s disease. Neurosci Biobehav Rev 2019; 103: 305-15.